Glioblastoom
synoniem
Glioblastoma multiforme
invoering
De Glioblastoom is de meest voorkomende kwaadaardige Hersentumor bij volwassenen, vanwege de zeer slechte prognose volgens de WHO-classificatie van primaire tumoren van de Centraal zenuwstelsel als de meest ernstige graad, dus een Graad IV glioblastoom,
is geclassificeerd. Glioblastoom is een van de astrocytische tumoren (gliomen), die qua weefsel (histologisch) lijken op de cellen van het ondersteunende weefsel (gliacellen) van de hersenen. Gliomen ontstaan uit de voorlopercellen van de gliacellen en zijn daarom hersentumoren (primaire hersentumoren).

frequentie
Glioblastoom is de meest voorkomende kwaadaardige hersentumor bij volwassenen. De incidentie van hersentumoren in het algemeen is naar verluidt ongeveer 50 per 100.000 inwoners per jaar, van de primaire hersentumoren komen gliomen het meest voor, met 4 à 5 nieuwe gevallen per 100.000 inwoners en jaar. Het meest voorkomende glioom is glioblastoom met meer dan 50% en is goed voor ongeveer 25% van alle primaire hersentumoren. Het aantal nieuwe gevallen van glioblastoom is dus ongeveer 3 per 100.000 inwoners per jaar.
Het komt het vaakst voor tussen de 60 en 70 jaar. Er worden echter ook aanzienlijk jongere mensen getroffen. Mannen worden bijna twee keer zo vaak ziek als vrouwen. Glioblastomen zijn zeer zeldzaam bij kinderen. Gelukkig zijn hersentumoren zeldzaam in vergelijking met andere tumoren. Slechts ongeveer 2% van alle kankerpatiënten lijdt aan een hersentumor.
Voorkomen
Glioblastomen groeien overal in het centrale zenuwstelsel (CZS), maar meestal in de Cerebrum. Ze vertrekken van het deel van de hersenen dat uit zenuwvezels bestaat (witte materie). De tumoren groeien infiltrerend, meestal onder de hersenschors (subcorticale), maar kan ook de schors grijpen. Ze zijn te vinden in alle hersenkwabben, maar ook in de zogenaamde balk die de twee hersenhelften met elkaar verbindt (Hemisferen) verbindt. Een glioblastoom dat uit de staaf steekt (Corpus callosum) van beide kanten naar de voorste hersengebieden (Frontale kwabben) zal zich verspreiden Vlinderglioom gebeld. Als er sprake is van uitgebreide infiltratie van het hersenweefsel met aantasting van ten minste twee hersenkwabben, spreekt men van één Gliomatosis cerebri. Soms groeien glioblastomen ook langs het gewelf (Fornix), die onder de lat ligt, in de Thalamus en zelden ook in het midden Hersenstam.
Verschijning

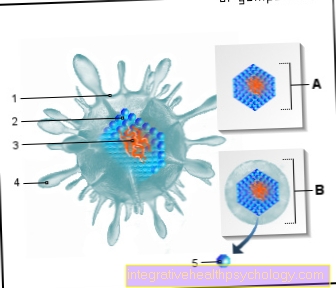
Microscopisch wordt het glioblastoom gekenmerkt door veelvormige (multiforme) cellen van verschillende grootte en vorm met eigenaardige kernen. Veel van de cellen bevinden zich in de celkernafdeling (mitose). De snelle groei van de tumor en het vrijkomen van een vaatvormende factor die door het tumorweefsel wordt geproduceerd, leidt tot de vorming van nieuwe abnormale (pathologische) bloedvaten met een defecte wandstructuur. Dit leidt tot verwijding van kleine bloedvaten (aneurysma's en varices), kortsluiting van slagaders en aders (arterioveneuze anastomosen) en zogenaamde "vroege aders". Dit leidt vaak tot bloeding (apoplectisch glioom) en ondervoeding van de tumor, wat leidt tot de dood van actieve cellen (necrose) in de tumor. Deze necrotische tumorgebieden zijn vaak omgeven door pseudopallisades, die bestaan uit lineair gerangschikte, nieuw gevormde (neoplastische) cellen.
Bovendien ontstaat er weefselzwelling als gevolg van de ophoping van vocht uit het vasculaire systeem rond de tumor (peritumoraal oedeem), wat vaak leidt tot zwelling van de hele hersenhelft.
oorzaken
Een glioblastoom kan primair zijn (meestal oudere patiënten), maar ook secundair vanwege de progressieve groei (progressie) van één Astrocytoom WHO-graad III doet zich voor (meestal patiënten van middelbare leeftijd). Astrocytomen ontwikkelen zich uit specifieke gliacellen, astrocyten genaamd, en behoren, net als glioblastomen, tot de groep van gliomen.
De rol van genetische factoren bij de ontwikkeling van Hersentumors komt de laatste jaren steeds meer naar voren. Het belangrijkste onderscheidende kenmerk van patiënten met secundair glioblastoom is een verandering in het p53-eiwit (p53-mutatie) dat de celcyclus regelt (tumoronderdrukker) en een verlies van genen (allelverlies) op chromosoom 17. Ze zijn ook 10 tot 20 jaar jonger dan patiënten met primair glioblastoom, waarbij er typisch een EGF-receptorgen-duplicatie (amplificatie) of een overmatige productie (overexpressie) van de EGF-receptor is. De EGF-receptor dient als een dokpunt voor de epidermale groeifactor (Epidermale groeifactor), dat fungeert als een signaalmolecuul in de celcyclus. Glioblastomen zijn genetisch zeer verschillend (heterogeen) en hebben een verlies van een gen (deleties) bij ongeveer 20% en genduplicaties bij ruim 50%. De meest voorkomende bevinding is een verlies van genen op chromosoom 10 in driekwart van alle gevallen.
Bij de meeste hersentumoren spelen genetische factoren echter geen rol. Ook omgevingsfactoren spelen slechts een ondergeschikte rol. Als voorbeeld van een beïnvloedende omgevingsfactor kan het vinylchloride in het kunststof PVC worden genoemd.Een erfelijke genetische factor kan worden waargenomen bij de zeldzame erfelijke ziekten Li-Fraumeni-syndroom en Turcot-syndroom. Glioblastomen komen hier in families voor.
Risicofactoren voor glioblastoom
De oorzaken van glioblastoom zijn niet volledig begrepen. De overgrote meerderheid van glioblastomen ontwikkelt zich spontaan, d.w.z. willekeurig. Een hoge blootstelling aan straling kan echter als risicofactor worden aangemerkt. Er zijn ook zeldzame genetische ziekten waarbij de getroffenen over het algemeen een verhoogd risico op tumoren hebben, b.v. de Li Fraumeni-syndroom. Ziekten van deze soort worden ook beschouwd als een risicofactor voor het ontwikkelen van glioblastoom. Bovendien is het niet ongebruikelijk dat hersentumoren van graad 3 in de loop van de tijd kwaadaardig worden en zo kan zich een glioblastoom (graad 4) ontwikkelen. Dit proces heet kwaadaardige progressie. Op basis van een andere hersentumor kan zelfs onder therapie een glioblastoom ontstaan. Men spreekt er dan in technische termen over secundair glioblastoom.
Symptomen
De eerste klinische symptomen verschijnen na enkele weken of eerder. hoofdpijn (35%), epileptische aanvallen (30%) en psychologische veranderingen (16%) zijn de meest voorkomende eerste symptomen. EEN verhoogde intracraniale druk veroorzaakt door het ruimtebesparende effect van de tumor en de daarmee samenhangende verstoring van de cerebrale stroom (vloeistofcirculatie) hoofdpijn, misselijkheid, Braken en zwelling (oedeem) van het uitgangspunt van de oogzenuw (congestieve papilla), wat kan leiden tot verminderd zicht. Verlamming kan ook optreden door de verspreiding van de tumor. Een aanval-achtige verslechtering van de symptomen is te wijten aan een bloeding van de tumor (apoplectisch glioom) en is niet ongebruikelijk.
U vindt meer informatie onder ons onderwerp: Hersentumor tekenen.
diagnose

Bij computertomografie (CT) worden glioblastomen gekenmerkt door verschillende dichtheden, wazige tumorgrenzen, centrale necrose binnen de tumor en groot oedeem rond de tumor (peritumoraal oedeem). Na toediening van het contrastmiddel, een stof die het beeldcontrast verhoogt, hoopt het contrastmiddel zich vooral op in de perifere zone van de tumor. Bij kleine tumoren wordt een ringstructuur zichtbaar, bij grotere een kransvorming. Tumorbloedingen komen voor bij ongeveer 7% van de glioblastomen.
In de MRI van de hersenen zie je de uitzaaiing van de tumor, deels over de lat. Na toediening van het contrastmiddel hoopt het contrastmiddel zich op in de vaste tumordelen. Het typische MRI-beeld van glioblastoom omvat ook restbloedingen en uitgebreid vingervormig peritumoraal oedeem. Het kan moeilijk zijn om het te onderscheiden van een grote, necrotische hersenmetastase en van een hersenabces.
Angiografie kan ook worden uitgevoerd, maar is niet langer een standaard bij de diagnose van glioblastomen. Contrastmiddel wordt in de bloedvaten geïnjecteerd en de bloedvaten worden weergegeven met behulp van diagnostische beeldvormingsmethoden zoals röntgenfoto's of MRI. Angiografie bij glioblastomen onthult in 60-70% van de gevallen een ophoping van het contrastmiddel in de pathologische vaten. De aderen die uit de tumor weglopen, worden al getoond tijdens de arteriële fase ("vroege aders"), waaruit blijkt dat het bloed te snel in de aderen stroomt via de arterioveneuze anastomosen.
Lees hier meer over angiografie
De uiteindelijke diagnose van het type tumor wordt in het weefsel gesteld (histologisch). Bij veel niet-operabele tumoren is histologische bevestiging van het type tumor vóór bestraling wenselijk. De hersenbiopsie, waarbij een heel klein stukje hersenweefsel wordt uitgesneden, wordt ofwel openlijk tegelijk met tumorreductie of onder lokale anesthesie minimaal invasief uitgevoerd, d.w.z. met de kleinste verwonding.
Mogelijk bent u ook geïnteresseerd in: Hersenbiopsie en Glioblastoom in het eindstadium
MRI van de hersenen - wat zie je?
Een glioblastoom wordt vaak vermoed met behulp van een beeldvormende test. Meestal is dit magnetische resonantiebeeldvorming. De typische bevinding toont een tumor zonder homogene (uniforme) structuur. De vaste delen (vaste delen) worden zeer goed van bloed voorzien en nemen daardoor veel contrastmiddel op. Dit is op het eerste gezicht duidelijk. Ze zijn erg helder en gloeien letterlijk op het MRI-beeld. Er zijn ook uitsparingen voor contrastmedium (gebieden die niet helder lijken op de MRI). Dit zijn cystische delen of aggregaten van dode cellen (necroses), deze worden niet aangevoerd door een bloedvat en kunnen daarom geen contrastmiddelen opnemen. De tumor wordt meestal direct gezien als een oedeem (gezwollen cellen). Het ruimteverslindende effect van de tumor kan vaak worden herkend bij de eerste diagnose, d.w.z. de middellijn is al verdrongen door de tumorgroei. Voor de definitieve diagnose moet echter een monster worden genomen en onder een microscoop worden onderzocht. Alleen de patholoog kan de diagnose glioblastoom met zekerheid bevestigen.
Lees meer bij: MRI van de hersenen
WIE - rang
De wereld Gezondheidsorganisatie (WHO) verdeelt hersentumoren in 4 groepen op basis van hun groeigedrag. Graad 1 tumoren groeien langzaam en worden als goedaardig beschouwd. Graad 4 tumoren groeien extreem snel en hebben een zeer slechte prognose. Graad 2 en 3 tumoren zitten er tussenin. EEN Glioblastoom is een tumor die afkomstig is uit de ondersteunende of envelopcellen van de zenuwcellen, dit wordt in vakjargon genoemd Gliacellen gebeld. Vandaar de naam. Vanwege de snelle groei en slechte prognose zijn glioblastomen graad 4 tumoren.
Graad 1 en 2
Hoewel tumoren van graad 1 door de WHO worden aangeduid als goedaardige hersentumoren, kunnen kwaadaardige cellen worden gedetecteerd in tumoren van graad 2. Bij 50% van de tumoren van graad 2 ontwikkelt zich een nieuwe tumor met een hoger maligniteitsniveau (graad 3-4), waardoor de levensverwachting ook beperkt is. Net als bij het gliobastoom zijn deze tumoren ook afkomstig van de ondersteunende of envelopcellen van de hersenen. In tegenstelling tot glioblastoom, een graad 4 tumor, groeien graad 2 hersentumoren veel langzamer en hebben ze een significant betere prognose.
Graad 3
Volgens de classificatie van de Wereldgezondheidsorganisatie (WHO) zijn graad 3-tumoren kwaadaardige, snelgroeiende hersentumoren. De prognose is slecht. Ondanks therapie overlijden veel patiënten na 2-3 jaar. Typische tumoren van graad 3 worden zo genoemd anaplastische astrocytomen; zoals de glioblastomen tegen hen vanuit de ondersteunende en envelopcellen van de zenuwcellen. Glioblastomen zijn echter door hun nog snellere groei een tumor van groep 4. Ondanks maximale therapie is de gemiddelde overlevingstijd ongeveer 1 jaar.
Graad 4
Graad 4 tumoren zijn zelfs nog kwaadaardiger, groeien sneller en leiden ondanks therapie tot een aanzienlijke vermindering van de levensverwachting. De indeling van de tumor in de overeenkomstige WHO-graad heeft dus een sterke invloed op de prognose van de patiënt. Glioblastomen zijn altijd graad 4 tumoren met een zeer slechte prognose. Uiteraard spelen ook andere factoren zoals operabiliteit, locatie en respons op chemotherapie en / of bestralingstherapie een belangrijke rol als het gaat om de prognose van de patiënt. De gemiddelde overlevingstijd voor glioblastoom is gemiddeld één jaar na diagnose.
Lees meer bij: Glioblastioom van graad 4
Levensverwachting / prognose
Helaas is glioblastoom erg moeilijk te behandelen. Een permanente genezing is meestal niet mogelijk. Uiteindelijk sterft de patiënt meestal aan de tumor. De standaardtherapie bestaat uit een operatie gevolgd door bestraling en chemotherapie. Helaas groeit de tumor erg snel en infiltreert hij in het omringende zenuwweefsel, zodat tijdens een operatie nooit alle tumorcellen kunnen worden verwijderd. De tumor komt meestal terug (Terugval). Met de volgende cijfers over prognose en levensverwachting moet men zich ervan bewust zijn dat dit statistieken zijn, in individuele gevallen kan de werkelijke overlevingstijd van de patiënt sterk variëren.
Jonge patiënten (leeftijd <50 jaar) met goede chirurgische resultaten hebben de beste prognose. 70% overleeft het eerste jaar. De mediane overlevingstijd na diagnose is 17-20 maanden. Slechts ongeveer 15 procent leeft na 5 jaar nog. De prognose verslechtert met de leeftijd. Bij patiënten ouder dan 50 jaar of bij jongere patiënten met aanzienlijke beperkingen is de gemiddelde overlevingstijd ondanks het goede chirurgische resultaat vaak iets minder dan een jaar. Bij patiënten zonder operatie of met een slechte neurologische functie postoperatief, is de prognose nog slechter. Slechts een derde overleeft het eerste jaar. Het gemiddelde sterft na 8 maanden. Individuele patiënten hebben ondanks terugval een relatief goede kwaliteit van leven en overleven desondanks meerdere jaren. Tot dusverre zijn dit echter geïsoleerde gevallen. Welke factoren de prognose gunstig beïnvloeden, wordt daarom intensief onderzocht.
Lees meer over het onderwerp: Glioblastoma - verloop van de afzonderlijke stadia
Hoe verloopt een glioblastoom?
Glioblastoom is een kwaadaardige tumor in de hersenen met een zeer slechte prognose. Genezing is meestal niet mogelijk. Patiënten overlijden gemiddeld ongeveer 1 jaar na de diagnose. Als de positie van de tumor gunstig is en de algemene toestand van de patiënt goed is, wordt eerst operatieve verwijdering uitgevoerd. Helaas groeit het glioblastoom zo infiltrerend in het zenuwweefsel dat nooit alle tumorcellen kunnen worden verwijderd. De operatie wordt daarom gevolgd door bestraling en chemotherapie. Dit kan echter alleen het natuurlijke verloop van de ziekte vertragen. Behalve in zeldzame individuele gevallen keert de tumor terug (Terugval). Het groeit meestal zo snel dat de verhoogde druk op de hersenen al snel symptomen veroorzaakt zoals misselijkheid / braken en hevige hoofdpijn. Bewustzijnsstoornissen volgen. De toenemende intracraniale druk houdt dan uiteindelijk bepaalde delen van de hersenen vast. Als de hersenstam wordt aangetast, zijn ademhalingsverlamming en de dood het gevolg. De bovenstaande behandeling kan dit enkele maanden uitstellen, maar het beloop van de ziekte is niet te stoppen en eindigt in de dood.
Lees meer over het onderwerp op: Verloop van een glioblastoom
Hoe ziet de eindfase eruit?
Glioblastoom is een kwaadaardige tumor waaraan patiënten gewoonlijk overlijden. Genezing is momenteel niet mogelijk - ondanks chirurgie, bestraling en chemotherapie. Uiteindelijk is het moeilijk vast te stellen wanneer het eindstadium is bereikt. Meestal groeit de tumor weer aan na de operatie (Terugval). Dit is vaak niet meer te bedienen. Soms is de tumor op het moment van diagnose zo groot of ongunstig gelokaliseerd dat er helemaal niet aan geopereerd kan worden. Als een tumor van graad 4 wordt glioblastoom gekenmerkt door snelle groei. In de laatste fase is de tumor erg groot. Er is echter maar een beperkte ruimte in de benige schedel. De druk op de hersenen neemt toe. Bij verhoogde intracraniële druk krijgen patiënten dan last van misselijkheid en braken, evenals ernstige hoofdpijn. Bewustzijnsstoornissen tot coma zijn mogelijk. Patiënten zijn vaak slaperig en verward. Door de toenemende intracraniale druk bestaat ook het risico dat bepaalde hersengebieden bekneld raken door te veel druk in de schedel, bijvoorbeeld als het ademhalingscentrum in de hersenstam wordt aangetast, ademhalingsverlamming en de dood optreden.
Lees meer over het onderwerp: Verhoogde intracraniale druk - tekenen, oorzaken en behandeling
Zoals bij de meeste kankers in het eindstadium, zijn patiënten vaak uitgemergeld door de lange duur van de ziekte. Je voelt je slap en uitgeput, het kan zijn dat je niet eens uit bed kunt komen. Men probeert dan het lijden enigszins te verlichten door de patiënt sterke pijnstillers voor te schrijven. De patiënt krijgt ook medicijnen tegen misselijkheid. EEN palliatieve zorg zou gedaan moeten worden.
Mogelijk bent u ook geïnteresseerd in: Glioblastoom in het eindstadium
Metastasen
Metastasen verspreiden de kanker door het hele lichaam. Men hoort ook vaak de woorden die de tumor heeft uitgezaaid. Men spreekt erover wanneer de tumor dochterknobbels heeft gevormd in een ander deel van het lichaam. Glioblastoom is een snelgroeiende kwaadaardige hersentumor. Het groeit infiltratief, d.w.z. het verspreidt zich zowel in de hersenen als in de hersenvliezen. Over het zenuwwater (Likeur) de tumorcellen zijn verdeeld over het centrale zenuwstelsel (hersenen en ruggenmerg) en kunnen zich overal weer nestelen. Dochtertumoren ontwikkelen zich zelden buiten het centrale zenuwstelsel.
Veranderingen in de natuur door de tumor
Elke kanker vertegenwoordigt een belangrijk keerpunt in het leven van de getroffen persoon. De verwerking van de diagnose glioblastoom verschilt sterk van persoon tot persoon, maar deze diagnose alleen al is een enorme psychologische last. De plotselinge confrontatie met het feit dat iemands leven eindig is, verandert de meeste mensen. Bovendien wordt de persoonlijkheid vooral in de hersenen opgeslagen in het voorste deel van de hersenen, de zogenaamde Frontale kwabben. Tumoren die daar groeien, kunnen leiden tot organische veranderingen in de natuur, omdat ze je eigen hersenweefsel verdringen. Helaas zijn patiënten meestal zonder reden agressief en beledigend. Dat is een enorme belasting voor het milieu. Door de toenemende intracraniale druk in het eindstadium van de ziekte zijn de patiënten doorgaans lusteloos en moe.
Kun je een glioblastoom genezen?
Helaas moet deze vraag met een duidelijk nee worden beantwoord. De mediane overlevingstijd na diagnose is één jaar. Uiteraard kan het individuele geval aanzienlijk verschillen van de statistieken. Vooral jonge patiënten (onder de 50 jaar) hebben een iets betere prognose. Ze overleven gemiddeld ongeveer 18 maanden. Er zijn ook geïsoleerde gevallen van patiënten die na 5 jaar nog in leven zijn. Het is mogelijk dat er een paar patiënten over de hele wereld zijn die 10 jaar na de diagnose nog in leven zijn, maar het is zeker de absolute uitzondering. Bij de huidige stand van de wetenschap is genezing van glioblastoom niet mogelijk. Er worden tal van onderzoeksbenaderingen gevolgd, maar tot nu toe is het onwaarschijnlijk dat in de komende jaren een dergelijke doorbraaktherapie zal worden ontdekt die tot genezing van de tumor zou kunnen leiden. In alle studies kon tot dusver alleen een toename van de overlevingstijd in maanden worden bereikt.
Wat is een multiform glioblastoom?
De term veelvormig betekent letterlijk "verschillend", D.w.z. gerelateerd aan de tumor, dat de tumor wordt gekenmerkt door een divers uiterlijk. Deze term komt van pathologie. Maar zelfs de onervaren arts kan op de MRI-opname al zien dat de tumor geen uniforme structuur heeft. Onder de microscoop zie je bloedingen en necrose (= dode cellen). Elk glioblastoom is per definitie een veelvormige tumor. Deze inhomogene (ongelijke) samenstelling kenmerkt het glioblastoom.
behandeling
De therapie bestaat uit de meest ingrijpende chirurgische verwijdering van de tumor en de daaropvolgende bestraling met een totale dosis van 60 Gray (30 individuele fracties - 2 Gy / 5 dagen / week gedurende 6 weken). Het oedeem reageert bijvoorbeeld goed op behandeling met steroïden Dexamethason, Aan. Met bestraling en anti-oedemateuze therapie kan aanvankelijk een klinisch indrukwekkende verbetering optreden. Een hernieuwd optreden of groei (terugval) van de tumor is onvermijdelijk. De belangrijkste prognostische factoren zijn: leeftijd en mate van klinische stoornis bij aanvang van de therapie.
Ook chemotherapie wordt steeds meer met de straling, vooral met de stof Temozolomide, gecombineerd of later gebruikt. Desalniettemin is de kans op therapie bij glioompatiënten laag, het overlevingspercentage na één jaar voor multiform glioblastoom is 30-40%. De chemotherapie met Nitreuze ureumverbindingen (BCNU, CCNU) leidt tot een lichte levensverlenging van slechts enkele weken tot maanden. Een alternatief voor de nitreuze urea is temozolomide, dat minder bijwerkingen heeft en poliklinisch kan worden toegediend als een oraal cytostaticum, een middel dat de celdeling remt. De combinatie van bestraling en chemotherapie met temozolomide leidt tot een verlenging van de levensduur tot 14 maanden (zonder temozolomide: 12 maanden) en een verhoogde tweejaarsoverleving van 26% (zonder: 10%). Jonge patiënten onder de 45 jaar met een goede gezondheid lijken het meeste baat te hebben bij deze therapie.
Temozolomide wordt ook gebruikt bij de behandeling van recidief van kwaadaardige gliomen. Terugval therapie leidt tot een stabilisatie van de tumorgroei bij ongeveer 50% van de patiënten en tot een totale overlevingstijd van 13 maanden na de start van de terugval therapie.
Wie kan er geopereerd worden?
Chirurgische verwijdering van een glioblastoom wordt beslist wanneer de tumor gemakkelijk toegankelijk en verwijderbaar is vanwege de locatie. Meestal zijn er al aanwijzingen voor de snelle groei van de tumor; men kan in de doorsnedebeeldvorming zien dat het omringende weefsel is verplaatst. Dit wordt een ruimteverslindend effect genoemd. Last but not least is de algemene toestand of het vermogen van de patiënt om te worden verdoofd doorslaggevend voor de beslissing om geopereerd te worden. Tumoren die te dicht bij belangrijke hersengebieden liggen, kunnen niet worden geopereerd. Als het spraak- of ademhalingscentrum zich bijvoorbeeld direct naast de tumor bevindt, is een operatie niet mogelijk of zinvol. Dan wordt de tumor geacht te zijn onbruikbaar.
Bestraling
Een operatie kan nooit alle tumorcellen verwijderen; geïsoleerde tumorcellen zijn nog steeds aanwezig. Deze kunnen weer uitgroeien tot een grote tumor. Om dit te voorkomen of in ieder geval zoveel mogelijk resterende tumorcellen te doden, volgt na de operatie bestraling. Niet alleen het oorspronkelijke tumorgebied wordt bestraald, maar ook een veiligheidsmarge van 2-3 cm. Soms krijgt de patiënt naast bestraling ook chemotherapie.
Lees meer over het onderwerp: Behandeling met bestralingstherapie
chemotherapie
Naast chirurgie en bestraling is chemotherapie de standaardtherapie voor glioblastomen. Doordat de tumor wekelijks in het hersenweefsel infiltreert, kunnen tijdens de operatie nooit alle tumorcellen worden verwijderd. Daarom kan chemotherapie de terugvalvrije overleving met ten minste een paar maanden verlengen. Temozolomide is het favoriete medicijn voor chemotherapie. Het is goed in het passeren van de bloed-hersenbarrière. Het is verkrijgbaar in tabletvorm en kan thuis worden ingenomen. Bovendien heeft het relatief weinig bijwerkingen en wordt het goed verdragen.
Immunotherapie
In de strijd tegen kwaadaardige tumoren nemen deze dagen toe Immunotherapeutica gebruikt. Maar wat betekent de term immunotherapie eigenlijk?
Immuuntherapie omvat het beïnvloeden van het eigen immuunsysteem van het lichaam met medicijnen om tumorcellen te doden. Het is eigenlijk een verzamelnaam voor tal van verschillende benaderingen. Glioblastoom is een zeer snelgroeiende kwaadaardige hersentumor die, ondanks maximale therapie, gepaard gaat met een zeer slechte prognose. Daarom is er veel hoop op immunotherapie. Er zijn ook veelbelovende benaderingen op dit gebied, die momenteel intensief worden onderzocht in klinische studies.
Methadon
Veel patiënten en familieleden hebben nu nieuwe hoop via berichtgeving in de media over methadon. Maar wat zijn de feiten? In het laboratorium is aangetoond dat methadon beter reageert op chemotherapie en dus effectiever wordt gedood.
Een studie uitgevoerd bij de Charité in Berlijn bij 27 patiënten kon echter geen enkel overlevingsvoordeel aantonen voor de met methadon behandelde groep. Andere collega's melden echter herhaaldelijk individuele gevallen waarin patiënten met methadon 2-3 jaar langer leven zonder recidieven. Het is daarom momenteel erg moeilijk om een aanbeveling te doen. Eerste laboratoriumresultaten en individuele casusrapporten spreken in het voordeel van methadon. Tot dusver zijn er echter geen hoogwaardige klinische onderzoeken met grote patiëntenpopulaties. Op deze gegevens kun je zeker pas over ongeveer 3 jaar rekenen. Voordien is het niet mogelijk om een wetenschappelijk onderbouwde uitspraak te doen over het belang van methadon bij kankertherapie. Getroffen patiënten hebben de mogelijkheid om met hun behandelende arts te bespreken of methadon wordt overwogen off-label therapie niettemin kan niet worden voorgeschreven in de zin van een experimentele genezingspoging. Een off-label therapie houdt in dat de arts de patiënt een medicijn voorschrijft, hoewel het niet is goedgekeurd voor de behandeling van een bepaalde ziekte. Methadon is een oud medicijn dat al heel lang is uitgeprobeerd en getest. Tot dusver is het echter niet goedgekeurd als aanvulling op chemotherapie voor glioblastoom, omdat er geen geldige gegevens zijn om de effectiviteit ervan te bewijzen.
Lees het volgende artikel voor meer informatie over het gebruik van methadon om verslaving te behandelen: Therapie van een verslaving
Wanneer heb je cortisone nodig?
Water afstotend (Oedeem) rond de tumor maken vaak deel uit van de ziekte, vooral in het eindstadium van glioblastoom. Dit leidt tot een zwelling van de zenuwcellen en verhoogt zo de intracraniale druk. Het zogenaamde hersenoedeem is een potentieel levensbedreigende ziekte. Cortison is nodig om hersenoedeem tegen te gaan. Het stabiliseert de celwanden, de cellen nemen niet meer ongecontroleerd vocht op en verliezen weer grootte. De hersenen zwellen op. Dit gebeurt binnen enkele uren na toediening van cortison. Daarom is cortison vaak een essentieel medicijn voor de patiënt.
epilepsie
De helft van alle patiënten met glioblastoom ontwikkelt ook epileptische aanvallen. De aanvallen kunnen soms zelfs het eerste teken zijn van de tumor die tot de diagnose leidt. Als de tumor vervolgens operatief wordt verwijderd, daalt het risico op aanvallen aanvankelijk aanzienlijk. In principe hebben patiënten met een hersentumor echter een significant verhoogd risico op epilepsie, dus na de eerste aanval moet beslist worden begonnen met medicamenteuze profylaxe om het risico op verdere aanvallen te verkleinen.
Lees meer over het onderwerp: Hersentumor tekenen
Is glioblastoom erfelijk?
Gelukkig kan deze vraag in de meeste gevallen met een volmondig nee worden beantwoord. Zelfs als een familielid, b.v. Als een van uw ouders een glioblastoom heeft ontwikkeld, loopt u geen groter risico om deze hersentumor te krijgen dan de algemene bevolking. Glioblastoom is een sporadische tumor, d.w.z. de tumor komt willekeurig voor, er is geen bewijs van erfelijkheid. Er zijn echter zeldzame genetische ziekten waarbij er in het algemeen een verhoogd risico is op kwaadaardige tumoren, b.v. de Li Fraumeni-syndroom of dat Turcot-syndroom. Glioblastomen kunnen natuurlijk ook vaker voorkomen in getroffen gezinnen.