Proteïne S-deficiëntie
definitie
Bij de Proteïne S-deficiëntie is het een aangeboren aandoening van het bloedstollingssysteem van het lichaamdie wordt veroorzaakt door een gebrek aan het anticoagulerende proteïne S. Deze ziekte heeft een prevalentie van ongeveer 0,7 tot 2,3% in de normale populatie nogal zeldzaam.

Proteïne S wordt meestal in de lever gevormd en zorgt er samen met andere anticoagulerende factoren voor dat a Bloedprop blijft beperkt tot de locatie van het vaatletsel.
Als dit eiwit een tekort heeft, overheersen de factoren die verantwoordelijk zijn voor de vorming van bloedstolsels, zodat het klinische beeld met bijvoorbeeld een verhoogde neiging om stolsels te vormen in intacte bloedvaten.
Patiënten lopen een verhoogd risico op een Veneuze trombose in het been of een veroorzaakt door een stolsel acute sluiting van een bloedvat.
Dit stolsel (trombus) kunnen ook vitale bloedvaten sluiten zodat a Tekort aan / onderaanbod van afhankelijke organen kan leiden tot weefselvernietiging, bijvoorbeeld in het hart, de longen, hersenen of darmen.
Zijn er verschillende vormen van de ziekte?
Het ziektebeeld van de patiënt is in principe onafhankelijk van de aanwezigheid van de verschillende subvormen. Men spreekt echter van drie subtypen, welke onderscheid diagnostisch te huur:
- Type I: Het is kenmerkend voor type I dat de activiteit van het aanwezige proteïne S wordt verminderd; maar ook de concentratie van het totale eiwit, evenals het vrije (actieve) eiwit in het bloed wordt verlaagd. Type I is per definitie aanwezig als de hoeveelheid vrij eiwit onder de 40% van de normale waarde komt.
- Type II: Van een type II-deficiëntie is sprake als alleen de activiteit van proteïne S wordt verminderd, maar de concentraties van zowel het totale als het vrije proteïne ongewijzigd blijven.
- Type III: Wijs de patiënt een normale concentratie van totaal proteïne S. aan, maar met een verminderde concentratie van vrij eiwit (<40%) en één Storing hiermee geassocieerd, lijden ze aan type III proteïne S-deficiëntie.
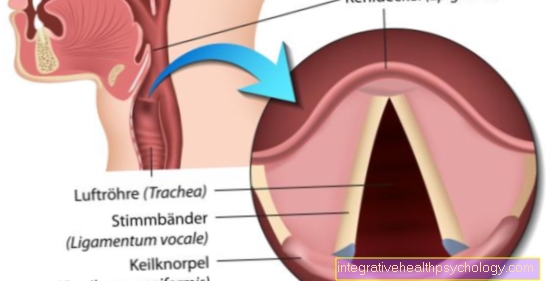
Algemene stolling
De bloedstolling verdeelt zich in de cellulair gedeelte, die wordt bereikt door het samenvoegen, netwerken en activeren van Bloedplaatjes (Bloedplaatjes) is in reliëf gemaakt, evenals de plasmatisch deelwaarbij bloedbestanddelen een soort netwerk vormen waarin circulerende rode bloedcellen (Erytrocyten) en stabiliseer het stolsel.
Bij gezonde mensen vormt zich pas een bloedstolsel nadat een vat is verwond; vezels (bestaande uit Collageen), welke buiten het vaartuig gelegen, blootgesteld aan de Verzamel bloedplaatjes en aldus een aanvankelijke, onstabiele sluiting van de wond teweegbrengen.
Deze bijlage (hechting) lost het Bloedplaatjes activering van waar naar Afgifte van verschillende stoffen, hoe Calcium en thromboxaanleidingen. Thromboxane ondersteunt het sluiten van de wond door een lokale vasoconstrictie; Calcium daarentegen is essentieel voor het functioneren van verschillende factoren in de plasmatische stollingsfase.
Als onderdeel van hun activering de bloedplaatjes veranderen ook hun structuur, zodat het oppervlak van de bloedplaatjes toeneemt en hun aggregatie een iets hogere stabiliteit heeft.
De ultieme stabiliteit van het stolsel alleen geborgd binnen de scope van de plasmatische component, waarbij door activering van de zogenaamde coagulatiecascade (bestaande uit diverse Vitamine K-afhankelijke factoren) Opslag van rode bloedcellen en de Verknoping van bloedplaatjes onder elkaar, de trombus wordt gestabiliseerd totdat de oorspronkelijke wond definitief is gesloten. In de context van wondgenezing is dit Bloedstolsels worden steeds meer afgebrokenzodat uiteindelijk het defect door nieuw vaatweefsel is gesloten.
Als er geen letsel is, kan het niettemin om bloedstolling te veroorzaken kom wat het lichaam effectief is voorkomen met behulp van een tegengesteld systeem kan; er is een constant evenwicht tussen stolselvorming en afbraak, die strikt wordt gecontroleerd.
De vorming van een stolsel wordt geremd door verschillende factoren die de effectiviteit van de trombusvorming verminderen en zo de vorming van een stolsel in een niet-verwond bloedvat voorkomen.
Deze factoren omvatten een complex bestaande uit Proteïne S en proteïne C, die samen een remmend effect op de stabilisatie van het primaire bloedstolsel Oefening in de plasmatische fase van bloedstolling.
Opgemerkt moet worden dat proteïne C in wezen aanwezig is in zijn actieve vorm en dus de remmende activiteit van de twee proteïnen alleen door activering en aggregatie met proteïne S. hangt er van af.
Als een patiënt lijdt aan een tekort aan proteïne S, is dit het geval Het remmende effect van proteïne S en proteïne C nam af of kan theoretisch geheel worden weggelaten, zodat de kans op trombusvorming groter wordt bij afwezigheid van vaatletsel.
Lees hier meer over het onderwerp: Bloedstolling
Symptomen
Meestal falen de patiënten vroege verschijning van veneuze bloedstolsels tussen de 15 en 45 jaar Aan.
Vooral vrouwen lijden onverwacht en zonder eerst van hun ziekte te weten trombose (Vasculaire occlusie door een bloedstolsel), opgehoopt in de diepe beenaders.
Dit gebeurt meestal in Risico situaties inclusief tijdens het nemen Oestrogenen (AnticonceptiepillenHormoonpreparaten voor menopauzeklachten) of zwangerschap aangezien deze ook verband houden met een afname van de proteïne S-concentratie.
Verder Risicofactoren Lijdt aan diepe veneuze trombose die beide geslachten in gelijke mate treft, zijn onder meer:
- Activiteiten,
- langdurige immobilisatie / immobilisatie van de benen na een operatie of tijdens een lange vlucht / busreis,
- zoals verhoogd vochtverlies.
diagnose

De ziekte kan alleen worden opgespoord door het bloed van de patiënt te analyseren. Als wordt vermoed dat een patiënt een verhoogde neiging tot stollen heeft, wordt gewoonlijk een veneus bloedmonster genomen en vervolgens een laboratoriumanalyse van de activiteit van de anticoagulerende factoren in het bloed, zoals proteïne S.
Hierbij moet onder meer worden opgemerkt dat proteïne S en de andere factoren slechts een korte halfwaardetijd hebben, d.w.z. hun activiteit kan alleen binnen een relatief kort tijdvenster worden gedetecteerd, zodat het belangrijk is om lange transportroutes naar een laboratorium te vermijden. Het verdient daarom aanbeveling deze onderzoeken te laten uitvoeren door een specialist met een aangesloten laboratorium of in een ziekenhuis.
Verder is de synthese van proteïne S en proteïne C ook vitamine K-afhankelijk, zodat medicatie met vitamine K-antagonisten (antagonisten) zoals bijvoorbeeld Marcumar tot onjuist lage waarden kan leiden.
Houd er ook rekening mee dat de concentratie van proteïne S bij vrouwen over het algemeen ongeveer twintig procent lager is dan bij mannen van dezelfde leeftijd en in verband met verhoogde oestrogeenspiegels (bijvoorbeeld bij het gebruik van de anticonceptiepil of hormoonpreparaten tijdens de menopauze), evenals tijdens en kan ook kort na de zwangerschap worden verminderd.
Daarom wordt een minimum interval van acht weken na de laatste inname van de vitamine K-antagonist en het einde van de invloed van oestrogeen aanbevolen.
behandeling
De ziekte is gebaseerd op één erfelijk genetisch defectwat de behandeling bemoeilijkt omdat het niet mogelijk is om de onderliggende oorzaak te behandelen.
De behandeling is dus vooral gebaseerd op de toestand van de patiënt, waarbij asymptomatische patiëntendie nog geen trombose hebben gehad geen permanente medicatie nodig hebben. In het geval van een hierboven beschreven risicosituatie, wordt u echter aangeraden om uw behandelend arts te informeren over de aanwezigheid van de ziekte, zodat er voldoende antistollingsmiddelen, zoals Heparine, kan gedaan worden.
Meestal blijven de patiënten onopvallend jarenlang en de ziekte zal pas na het optreden van een eerste trombose gediagnosticeerd.
Dit betekent echter dat therapie met een anticoagulans moet worden geadviseerd om de vorming van nieuwe bloedstolsels te voorkomen.
Omdat vitamine K nodig is voor de synthese van belangrijke stollingsfactoren, wordt het gebruik van vitamine K aanbevolen voor langdurige behandeling Vitamine K-antagonisten (antagonist = Tegenstander), zoals Marcumar, Aan. Deze verdringen vitamine K uit de synthese van de factoren die nodig zijn voor plasmatische coagulatie, zodat het gebrek aan remmende werking van proteïne S en C niet langer "significant" is.
Als u een bekend proteïne S-tekort heeft bij zwangere vrouwen wordt een nadere observatie en indien nodig behandeling met anticoagulantia, aanbevolen tijdens de zwangerschap om het risico op trombose en daarmee samenhangend te verminderen Zwangerschapscomplicaties vermijden.
Hoe wordt de ziekte overgeërfd?

Omdat de ziekte niet erfelijk is, is deze gekoppeld aan de geslachtschromosomen Getroffen vrouwen en mannen in gelijke mate.
Verder spreekt men van een dominante overerving, aangezien een verandering in slechts één van de twee verantwoordelijke genen leidt tot de expressie van de deficiëntie.
De waarschijnlijkheid Als gevolg hiervan komt ook het hebben van de genetische eigenschap van proteïne S-tekort voor bloedverwanten in de eerste graad Getroffen (Ouders, kinderen, broers en zussen) 50 procent. Omdat het tekort echter niet automatisch gepaard gaat met het ontstaan van trombose, veel patiënten herkenden pas na decennia.
Is de aanwezigheid van een Bekend om gebrek binnen het gezin, kan een Onderzoek van familieleden in de eerste graad, vooral vrouwelijke familieleden in de vruchtbare leeftijd of voordat therapie met oestrogenen (vrouwelijke geslachtshormonen) nuttig kan zijn. Een onderzoek verloopt meestal zonder problemen vanaf de zesde levensmaand mogelijk, hoewel "screeningsonderzoeken" in het algemeen achterwege blijven als er een geval binnen de familie bekend is.
Profylaxe voor de getroffenen
In vergelijking met andere ziektebeelden is in de context van een speciaal dieet tot dusver geen positieve invloed op het anticoagulans waarneembaar.
Artsen bevelen echter aan in aanwezigheid van erg overgewicht een Verandering van dieet op een gezond, vitaminerijk, mogelijk mediterraan geïnspireerd dieet met als doel een algemeen gewichtsverlies. Dit heeft in principe een positief effect op het cardiovasculaire systeem, maar heeft geen specifiek preventief voordeel in de context van een proteïne S-deficiëntie.
Tot een trombose moet worden voorkomen regelmatige lichaamsbeweging zo goed als dat Het dragen van steun- / steunkousen vooral in risicovolle situatieshoe typisch een lange vlucht / busreis, sterk aanbevolen.
Heeft de betrokken persoon heeft al een trombose gehad, dit zou moeten zijn Volg strikt de instructies van uw arts, en neem gewetensvol voorgeschreven medicijnen om herhaling te voorkomen. Om het optreden van een veel voorkomende complicatie van een eerdere trombose (de zogenaamde P.Oostelijk trombotisch syndroom) om dit tegen te gaan, moet de patiënt draag dagelijks compressiekousen.